Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Caldasia
versión impresa ISSN 0366-5232versión On-line ISSN 2357-3759
Caldasia v.29 n.2 Bogotá jul./dic. 2007
RELACIÓN ENTRE LA DIVERSIDAD DE ANUROS Y LOS ESTADOS SUCESIONALES DE UN BOSQUE MUY HÚMEDO MONTANO BAJO DEL VALLE DEL CAUCA, SUROCCIDENTE COLOMBIANO
Relationship between anurans diversity and sucesional stages of a very humid low montane forest in Valle del Cauca, southwestern, Colombia
JUAN CARLOS GARCÍA-R.
HEIBER CÁRDENAS-H.
FERNANDO CASTRO-H.
Maestría-Biología, Universidad del Valle, Cali, Colombia. juacagar@yahoo.com
Universidad del Valle, Departamento de Biología, Cali, Colombia. hecarden@univalle.edu.co; fcastro@univalle.edu.co
RESUMEN
Se examinó la relación de parámetros vegetales y variables climáticas con la distribución y la abundancia de anuros en un bosque muy húmedo montano bajo del occidente del Valle del Cauca, Colombia. Se muestrearon durante siete meses seis transectos en tres tipos de hábitat (bosque secundario, bosque secundario temprano y matorral). Se obtuvieron datos de las características del bosque (cobertura, alturas promedias y densidades de diferentes estratos, profundidad de la hojarasca, temperatura del aire, temperatura del suelo y humedad relativa) en cada sitio. Se registraron cinco especies del género Pristimantis y una del género “Eleutherodactylus”, siendo la más abundante P. brevifrons con un total de 19 individuos, seguida de P. palmeri con 15 y P. erythropleura con 14. La distribución de las especies presentó diferencias significativas entre los hábitats y las variables climáticas. La abundancia de las especies en el bosque secundario estuvo correlacionada con la temperatura del suelo, y en bosque secundario temprano y matorral con la humedad relativa. De acuerdo con los aspectos estructurales de la vegetación, se sugiere la existencia de tres comportamientos diferentes dentro del grupo de anuros respecto a los siguientes parámetros: cobertura vegetal (%), altura promedio (m) del estrato subarbóreo (Ar), densidad de este estrato (ind/m2), densidad (ind/m2) del estrato arbustivo (ar) y la profundidad de la capa de hojarasca (cm). Por lo tanto, se observan tres grupos de especies aparentemente diferentes, definidos según los siguientes criterios: el grupo I, constituido por especies que toleran más los ambientes medianamente intervenidos (P. brevifrons, P. erythropleura, “E”. mantipus); el grupo II, cuyas especies se encuentran presentes en ambientes más conservados (P. calcaratus, P. thectopternus); y el grupo III conformado por P. palmeri, presente en ambientes mediana y altamente intervenidos.
Palabras clave. Anura, bosque de niebla, Fauna de Colombia, Pristimantis, parámetros vegetales, variables climáticas.
ABSTRACT
We examined the relationship of climatic variables and vegetation parameters with the distribution and abundance of anurans in a very humid low montane forest in the western region of Valle del Cauca, Colombia. We sampled six transects in three types of habitat (secondary forest, early secondary forest and shrub area), over a period of seven months. We collected data on several forest characteristics (vegetation cover, average heights and densities of different strata, depth of leaf litter, air temperature, soil temperature and relative humidity) in each site. Five species of genus Pristimantis and one of genus “Eleutherodactylus” were registered being the most abundant (P. brevifrons with a total of 19 individuals, followed by P. palmeri with 15 and P. erythropleura with 14). The distribution of species differed between habitats and climatic variables. The abundance of the species in the secondary forest was correlated with the soil temperature, whereas relative humidity was correlated with species abundance in early secondary forest and shrub. We suggest the existence of three different behaviors within the group with respect to the following structural parameters: vegetation cover (%), average height (m) of the subarboreal (Ar) stratum, density of this stratum (ind/m2), density (ind/m2) of the bush stratum (ar) and thickness of the leaf litter layer (cm.). We identify three groups of species defined according to the following criteria: group I, comprised of those species that tolerate moderately degraded environments (P. brevifrons, P. erythropleura, “E”. mantipus); group II, present in more conserved environments (P. calcaratus, P. thectopternus); and group III comprised by P. palmeri, which is present in medium to highly degraded environments.
Key Words. Anura, climatic variables, cloud forest, Fauna of Colombia, Pristimantis, vegetation parameters.
INTRODUCCIÓN
Desde finales de la década de 1980 se ha documentado la desaparición repentina de un gran número de poblaciones de anfibios en varios sitios de Estados Unidos de América, Centro y Sudamérica, Europa y Australia (Donnelly 1998). Se ha sugerido que esta declinación puede deberse a factores relacionados con la acción sinérgica de agentes de disturbio como la contaminación, el cambio de uso de la tierra, la introducción de predadores y competidores no nativos, el calentamiento global, al igual que a pandemias y/o fenómenos naturales (Pounds & Crump 1994, Lips 1998, Young et al. 2001, Collins & Storfer 2003, Pounds et al. 2006). Sin embargo, para poder reconocer las causas locales o globales responsables de este fenómeno, deben considerarse la realización de estudios a largo plazo que provean información confrontable y comprobable de parámetros indicadores del estado de las poblaciones tales como su distribución y abundancia, el rango de condiciones bajo las cuales viven y cómo éstas fluctúan con las variables ambientales (Donnelly 1998, Parris 1999).
Diversos estudios señalan la importancia de variables del hábitat en la organización de comunidades animales como insectos, aves, anfibios y lagartos, entre otros (véanse Karr & Roth 1971, Castro 1988, Pearman 1997, Camero 1999). En Colombia, los estudios que involucran la relación entre anuros y el hábitat se enfocan en la distribución y la estructura de las comunidades en zonas con diferentes estados sucesionales (e.g. Rincón & Castro 1998, Vargas & Castro 1999, Vargas & Bolaños 1999), pero pocas de estas investigaciones evalúan las variables físicas y vegetales que posiblemente determinan la selección del hábitat por este tipo de fauna (e.g. Urbina & Londoño 2003, García et al. 2005).
La fragmentación del bosque puede afectar a las poblaciones de anuros a raíz de los cambios en la calidad del hábitat. La relación entre el hábitat y las especies de anuros es importante, ya que estas últimas son influenciadas en gran parte, directa o indirectamente, por el grado de alteración o manipulación de las áreas que ocupan y el comportamiento asociado de diversos elementos microclimáticos, lo cual las convierte por consiguiente, en indicadoras de la salud ambiental de los ecosistemas (Blaustein & Wake 1995). Es decir, que de acuerdo con el tipo de vegetación, las condiciones físicas y el grado de perturbación de los hábitats podrían encontrarse variaciones en los atributos y la estructura de las comunidades de anuros.
El conocimiento de la asociación entre la diversidad de anuros y las variables bióticas y abióticas del hábitat es esencial para el manejo y la conservación local de bosques y ranas. Este estudio se realizó en un bosque de niebla del occidente colombiano en donde se evaluó la relación de las características del hábitat (aspectos fisionómicos de la vegetación, datos climáticos y de microhábitat) con la distribución y las propiedades emergentes de los anuros a través de estaciones espaciales con diferentes grados de perturbación para responder a las siguientes preguntas: 1) ¿existe diferencia en la diversidad de especies entre los hábitats?, 2) ¿cuáles son los microhábitats y actividades más frecuentes en las especies de anuros?, y 3) ¿cuál es la relación entre las variables ambientales y las comunidades de anuros?.
MATERIALES Y MÉTODOS
Área de estudio
Este estudio se llevó a cabo en el Ecoparque “Bosque de Niebla” ubicado en el condominio Villas de Loma Alta (3º 30’ 39’’ Norte y 76º 38’ 06’’ Oeste) de la vereda Loma Alta, municipio de Dagua (Valle del Cauca, Colombia), a 4 km de lo que se conoce como “el dieciocho” (kilómetro 18 vía al mar, de la carretera que de Cali conduce a Buenaventura). Esta zona está ubicada en el flanco oriental de la Cordillera Occidental y se caracteriza por presentar fragmentos de bosque en diferentes estados sucesionales entre una matriz de pequeñas fincas y hábitats suburbanos.
La altitud de la zona varía entre 1600 y 2000 m sobre el nivel del mar, con una temperatura promedio de 16 oC y una precipitación promedio anual de 1600 mm/año, con dos picos de lluvias en los meses de abril-mayo y octubre-noviembre, según los registros de la estación de San Pablo. Esta región pertenece, conforme a la clasificación de Holdridge (1996), a un bosque muy húmedo montano bajo (bmh-MB).
La comunidad de la Vereda Loma Alta está constituida por campesinos, cuya principal actividad económica es la agricultura y la ganadería a menor escala. La mayoría de cultivos son de tipo extensivo (baja tecnología en cuanto a maquinaria y uso en gran cantidad de agroquímicos), siendo más frecuentes los de yuca, maíz, lechuga, arracacha, plátano, flores y plantas aromáticas.
Método y unidades de muestreo
El Muestreo por Encuentros Visuales (Visual Encounter Survey, VES) es una técnica utilizada en el inventario y/o monitoreo de anfibios para determinar la riqueza de especies en un área y estimar las abundancias relativas de las especies en un ensamblaje (Crump & Scott 1994). En este estudio, se empleó el método VES con el muestreo en transectos. Se establecieron seis transectos (dos por cada tipo de hábitat) de 50 m de largo y 1 m de ancho a cada lado en tres tipos de hábitat, muestreados una vez por mes durante siete meses (nov 2002, feb-mar-abr-jul-nov 2003 y ene 2004). El tipo de muestreo fue estratificado con localización al azar de los transectos en una franja altitudinal entre 1700-1800 msnm.
La escogencia de los sitios de muestreo fue determinada por las diferencias en su fisonomía vegetal: a) BOSQUE SECUNDARIO (BS): zona protectora de una quebrada, poco intervenida, caracterizada por elementos florísticos representativos de los bosques montanos, especies de las familias Moraceae y Rubiaceae presentes en casi todos los estratos, y gran porcentaje de cobertura arbórea. b) BOSQUE SECUNDARIO TEMPRANO (BST): zona en estado transicional temprano, con aproximadamente 15 años de recuperación; área muy homogénea donde es común vegetación de estratos arbustivo y subarbóreo, predominando especies de la familia Melastomataceae. c) MATORRAL (M): zona en recuperación cuya vegetación se limita a los estratos herbáceo y arbustivo dominados por helechos.
Captura e identificación de especies
Se efectuaron observaciones continuas con jornadas de trabajo en la mañana (09:00 – 12:00 h) y en la noche (19:00 – 23:00 h). Si el muestreo en la mañana no era posible, éste se realizaba en la tarde entre las 14:00 – 17:00 horas, pero teniendo en cuenta que los seis transectos fueran muestreados en la misma jornada y el mismo día. En cada transecto se capturaron manualmente los individuos localizados hasta una altura de dos metros.
La identificación de los individuos se realizó en el campo y éstos fueron liberados después de la toma de los siguientes datos: a) Fecha y hora de captura, b) Transecto evaluado, c) Especie, d) Altura en la que fue encontrado el individuo o Distancia Vertical (I = 0-40 cm; II = 41-80 cm; III = 81-120 cm; IV = 121-160 cm; V = 161-200 cm), e) Sustrato sobre el que fue hallado (Hojas (H); Hojarasca (HOJ); Roca (RC); Tronco (TR); Rama (RM); Musgo (MG)), f) Distancia de la fuente de agua permanente más cercana o Distancia horizontal (1 = 0-2.5 m; 2 = 2.5-5 m; 3 = 5-7.5 m; 4 = 7.5-10 m; 5 = >10.0 m) y g) Actividad del individuo (perchado, cantando, amplexo, oviposición, alimentándose o saltando).
Determinación de las variables del hábitat
Las variables físicas medidas en los transectos de muestreo fueron: Altitud (msnm) y Pendiente (grados) (medidas con un altímetro y un clinómetro, respectivamente). Temperatura del aire (°C) (TA), Temperatura del suelo (°C) (TS) y Humedad relativa (%) (HR), donde la temperatura del aire y la humedad relativa se midieron mediante con un higrotermómetro (OAKTON 35700-00) a una altura de 150 cm del suelo, y la temperatura del suelo se midió con un termómetro manual diseñado para este tipo de evaluación (“soil test” TAYLOR 5976). Las mediciones se realizaron cada vez que se condujo el monitoreo de los transectos.
La evaluación sobre aspectos estructurales de la vegetación se realizó en un transecto de 50 m x 2 m en cada tipo de hábitat. Los datos obtenidos fueron los siguientes: a) Altura promedio del estrato arbóreo, subarbóreo y arbustivo (m). Para la estratificación de la comunidad vegetal, se tomó en cuenta la propuesta de Rangel y Lozano (1986), que contempla los siguientes intervalos: estrato rasante (r): 0-0.25 m; estrato herbáceo (h): 0.25-1.5 m; estrato arbustivo (ar): 1.5-5 m; estrato subarbóreo o de arbolitos (Ar): 5-12 m; estrato arbóreo inferior (Ai): 12-25 m, y estrato arbóreo superior (As): >25 m; b) Cobertura vegetal (%), que se estimó a través de un densiometro esférico cóncavo, por el cubrimiento del área que proyectan sobre la superficie del transecto las copas de las plantas; c) Densidad de individuos en el estrato arbóreo, subarbóreo y arbustivo (número de individuos/m2), que se evaluó por conteo directo de los individuos ubicados en los estratos arbóreo, subarbóreo y arbustivo (Rangel y Velásquez 1997); teniendo en cuenta sólo los individuos con Circunferencia a la Altura del Pecho, CAP > 2.5 cm; d) Profundidad de la capa de hojarasca (cm), donde se efectuó un cálculo del promedio de la profundidad de la capa de hojarasca a través de cinco puntos al azar dentro del transecto.
Análisis de datos
Se hicieron pruebas de Chi cuadrado para establecer la existencia de diferencias significativas en la distribución vertical de las especies eleutherodactylinas dentro del bosque. Igualmente, se diseñaron tablas bifactoriales entre la distancia vertical y la actividad y entre distancia vertical y sustrato. Se efectuó una prueba de homogeneidad dentro de las especies agrupadas según su cercanía o no a la fuente de agua permanente para determinar si existe diferencia entre estos grupos respecto a su distribución horizontal. Para conocer el aporte de los factores distribución vertical y distribución horizontal a la varianza total de la abundancia de las especies se realizó un ANOVA de dos factores sin repetición (Sokal & Rohlf 1969).
Para comprobar la hipótesis de que las muestras proceden de tres hábitats diferentes se realizó una prueba de medianas, dado que existen algunos datos extremos que pueden afectar el indicador de tendencia central. En este caso la probabilidad de obtener una Temperatura del Aire < a la mediana, es la misma en todos los hábitats. Igual prueba se realizó comparando las Temperaturas del suelo y la Humedad relativa en cada hábitat. Estas pruebas también se realizaron para asociar la distribución de las especies a los hábitats y a las variables climáticas.
Se realizaron correlaciones de Pearson entre las variables climáticas de los hábitats con respecto a las abundancias de las especies de ranas, y regresiones cuadráticas entre las variables climáticas para predecir los valores de mayor captura, y la distancia horizontal (distancia a una fuente de agua) y la abundancia de individuos. Para determinar la relación entre la abundancia de las especies de ranas y la estructura vegetal de los hábitats se llevo a cabo una prueba de Chi cuadrado. Para los análisis fueron utilizados los programas Statistica v.6.0 (StatSoft 2001) y Excel (Microsoft Office 2003).
RESULTADOS Y DISCUSIÓN
Estructura y composición de anuros
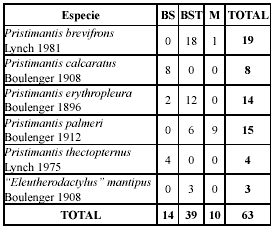
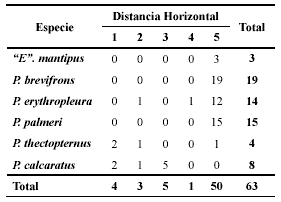
Durante el período de estudio se registraron 63 individuos pertenecientes a seis especies, cinco incluidas en el género Pristimantis y una en el género “Eleutherodactylus” (sensu Heinicke et al. 2007). Entre las especies capturadas más abundantes se encontraron Pristimantis brevifrons con 19 individuos (30%), Pristimantis palmeri con 15 (24%) y Pristimantis erythropleura con 14 (22%). Los miembros del género Pristimantis y “Eleutherodactylus”estudiados mostraron preferencia por el hábitat Bosque Secundario Temprano (BST), ya que el 62 % de los individuos fueron capturados en este ambiente. En el Bosque Secundario (BS) se observó el 22%, y el restante 16% fue observado en Matorral (M). En la Tabla 1 puede observarse que Pristimantis calcaratus y Pristimantis thectopternus se hallaron sólo en el BS y “Eleutherodactylus” mantipus se halló sólo en el BST. Pristimantis brevifrons y P. palmeri no se registraron en el BS, pero mientras la primera presentó mayor preferencia por el BST (95%) que por M (5%) la segunda no señaló tal particularidad (BST = 40%; M = 60%). Pristimantis erythropleura, al igual que P. brevifrons, mostró mayor preferencia por el hábitat BST (86%) que por el BM (14%), pero nunca se registró en M. De las especies registradas una se encuentra En Peligro (EN) (P. calcaratus), y las demás en Preocupación Menor (LC) de acuerdo con las categorías de la lista roja del UICN.
Tabla 1. Especies y número de individuos registrados en cada hábitat estudiado (BS = Bosque Secundario, BST = Bosque Secundario Temprano, M = Matorral).
Microhábitat y actividad
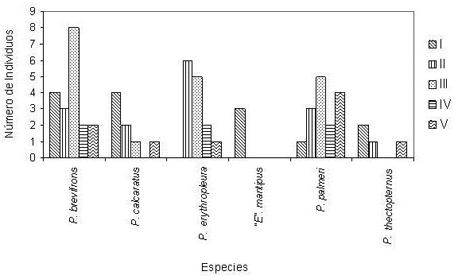
El 94% de los individuos se registraron en la noche. Las únicas especies registradas en los muestreos diurnos fueron “E”. mantipus (66% de los individuos) y P. brevifrons (11%). Con respecto a la distribución vertical dentro del hábitat se establecieron dos agrupaciones de acuerdo a la similitud en las abundancias y presencia/distribución en las clases de altura, sin observar diferencias significativas entre las especies que las conformaron (Grupo I: X 2 = 3.4; P = 0.9040 y Grupo II: X 2 = 8.8; P = 0.3556), dando como resultado que el 60% de los individuos entre las especies “E”. mantipus, P. calcaratus y P. thectopternus (Grupo I) se localizaron en la distancia vertical I (0-40 cm) y el 20% en alturas mayores a la distancia vertical III, es decir a más de 120 cm. Por el contrario, entre las especies restantes (P. brevifrons, P. erythropleura y P. palmeri = Grupo II) solamente se halló el 10% de los individuos en la distancia vertical I (0-40 cm) y aproximadamente el 65% a distancias mayores de 120 cm (Figura 1).
Figura 1. Distribución de los individuos de las especies eleutherodactylinas con respecto a las clases de altura. Donde: I (0 – 40 cm), II (41 – 80 cm), III (81 – 120 cm), IV (121 – 160 cm) y V (161 – 200 cm).
En cuanto al comportamiento de los individuos en el momento de su captura, el 74.6% fueron hallados perchados, mientras un 12.7% fueron registrados vocalizando, 3.2% en amplexo y 9.5% saltando. No se observó a ningún animal alimentándose en el momento de captura (Tabla 2). Estos datos son comunes para el grupo de acuerdo con Lynch & Duellman (1997), quienes afirman que la mayoría de las veces estas ranas se perchan sin hacer nada, en un comportamiento sedentario típico de predadores de sentarse y esperar, aunque los machos de algunas especies también vocalizan. El amplexo señalado en la Tabla 2 corresponde a un apareamiento observado en el mes de julio de 2003 para la especie P. palmeri. Adicionalmente, para las especies de Loma Alta, cuando se consideran las actividades canto y amplexo como una sola actividad reproductiva, y aparte se considera el perchado para el análisis, no se observan diferencias significativas para estas actividades en su distribución con respecto a la distancia vertical (X 2 = 5.1; P = 0.2762).
Tabla 2. Actividad de los individuos en el momento de captura respecto a la distancia vertical. Donde: I (0 – 40 cm), II (41 – 80 cm), III (81 – 120 cm), IV (121 – 160 cm) y V (161 – 200 cm).
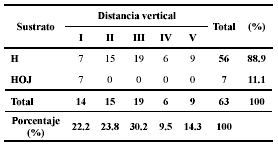
El 89% de los individuos perchan en hojas y el 11% restante se encuentran en hojarasca. A diferencia de lo afirmado por Lynch & Duellman (1997) ningún individuo fue observado en ramas. El 85.7% de los individuos se sitúan en un rango de alturas dentro del hábitat entre 0 y 1.6 m lo que coincide con las frecuencias de observaciones de estos autores para el grupo. Solamente en la distancia vertical I (= 40 cm) no se observó preferencia por hojas (Tabla 3).
Tabla 3. Distribución estructural del microhábitat por los individuos de las seis especies estudiadas de eleutherodactylinos. Donde: I (0 – 40 cm), II (41 – 80 cm), III (81 – 120 cm), IV (121 – 160 cm), V (161 – 200 cm), H (Hojas) y HOJ (Hojarasca).
Para el grupo de especies, se observó que la mayoría de los individuos se distribuyeron a distancias superiores a 10 m de una corriente de agua permanente (50/63=79.3%). En la Tabla 4 se observa que a nivel de especie existen dos agrupaciones; la primera está conformada por “E”. mantipus, P. brevifrons, P. erythropleura y P. palmeri, donde la mayoría de sus individuos se ubican a más de 10 m. (49/51=96%). La segunda agrupación la conforman P. thectopternus y P. calcaratus, especies que se encuentran a distancias menores de 10 m de la fuente de agua (11/12=91.7%). Las pruebas de homogeneidad dentro de cada grupo, no manifestaron diferencias significativas entre las especies que los conforman (Grupo I: X 2 = 5.5; P = 0.4813; Grupo II: X 2 = 5.25; P = 0.1544).
Tabla 4. Distribución horizontal o distancia respecto a la fuente de agua permanente de los individuos de las especies estudiadas. Las distancias (m) fueron: 1 (0.0 – 2.5), 2 (2.5 – 5.0), 3 (5.0 – 7.5), 4 (7.5 – 10.0) y 5 (>10.0).
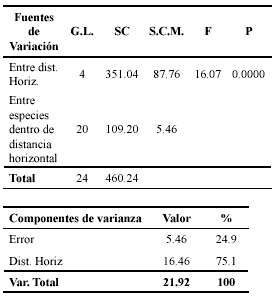
Al hacer un análisis de varianza de dos factores sin repetición en donde uno de los factores considerados es la distancia horizontal y el otro, la distancia vertical, se observó que el efecto del factor distancia horizontal sobre la varianza total de la abundancia de especies del grupo de estudio tuvo un peso del 78% (P<0.0001), mientras que el efecto del factor distancia vertical no fue significativo (P=0.3442). Por esta razón, la Tabla 5 muestra el ANOVA y el componente de varianza del factor significativo.
Tabla 5. Análisis del factor distancia horizontal sobre la abundancia de las seis especies estudiadas. En esta tabla también se indican los componentes de la varianza total.
En la Figura 2 se muestra una regresión cuadrática significativa (R2 =0.62; F=52.63; P<0.0001) entre la distribución horizontal (m) y la abundancia (No. de individuos registrados). Se observa para este grupo de ranas eleutherodctylinas, en general, que la frecuencia de individuos aumenta a medida que se alejan de la fuente de agua permanente, posiblemente debido a que sus especies no necesitan de ella directamente sino de una alta humedad para su reproducción y desarrollo, pues no se congregan en sitios de reproducción y sus huevos son puestos sobre la hojarasca.
Figura 2. Regresión cuadrática entre la distribución horizontal (m) y la abundancia (No. de individuos registrados). (R2 = 0.62; F = 52.63; P<0.0001).
Características del hábitat ocupado
La Temperatura del Aire en los sitios varío entre 15.5 y 18.4 °C, la Temperatura del Suelo entre 15.0 y 20.0 °C, ésta última registrada en Matorral, y la Humedad Relativa entre 74 y 100%, ambas encontradas en BST (Tabla 6).
Tabla 6. Variables climáticas medidas en los hábitats de estudio en un Bosque de Niebla del occidente colombiano.
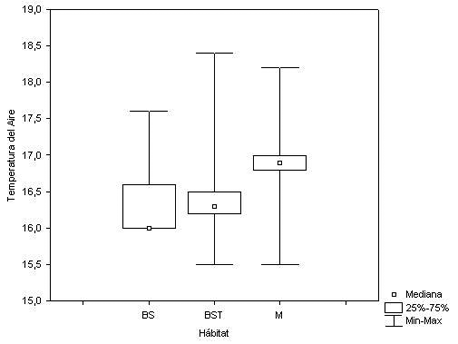
Se determinó si existen diferencias significativas entre cada hábitat estudiado respecto a las variables climáticas TA, TS y HR llevando a cabo pruebas de medianas. La prueba de Chi cuadrado para saber si existe diferencia entre las Temperaturas del aire en los hábitats estudiados resultó significativamente diferente (X 2 = 10.14, P = 0.0063) (Figura 3).
Figura 3. Temperatura del Aire (TA) según el hábitat estudiado. Donde: BS = Bosque Secundario, BST = Bosque Secundario Temprano, y M = Matorral.
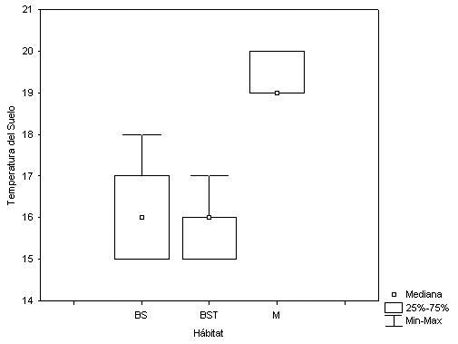
La prueba realizada comparando las Temperaturas del suelo y la Humedad relativa en cada hábitat reveló igualmente diferencias significativas (X 2 = 37.37, P < 0.0001; X 2 = 22.65798, P < 0.0001, respectivamente) (Figura 4 y Figura 5).
Figura 4. Temperatura del Suelo (TS) según el hábitat estudiado. Donde: BS = Bosque Secundario, BST = Bosque Secundario Temprano, y M = Matorral.
Figura 5. Humedad Relativa (HR) según el hábitat estudiado. Donde: BS = Bosque Secundario, BST = Bosque Secundario Temprano y M = Matorral.
Se realizó una prueba de Chi cuadrado para saber si las especies se distribuyen independientemente del hábitat y se observó que presentan diferencias significativas en la distribución de acuerdo con los hábitats (P < 0.0001). Igualmente, existen diferencias significativas en la presencia de las especies de acuerdo con las variables climáticas (TA = X 2 = 12.36407, P = 0.0301; TS = X 2 = 25.34606, P = 0.0001; HR = X 2 = 15.41203, P = 0.0087).
Al analizar la abundancia con las variables climáticas se encuentra que para BS existe una correlación lineal negativa altamente significativa (R2=0.77; P=0.0094) con la temperatura del suelo. Lo cual quiere decir que a mayor temperatura del suelo hay una menor abundancia de individuos. En BST y M existe una tendencia lineal que indica que a mayor humedad relativa mayor abundancia de individuos (BST: R2=0.51; P=0.07; M: R2=0.47; P=0.08). Cuando se analizó esta correlación en BST para las especies más abundantes en este hábitat se observó que para P. erythropleura es altamente significativa (R2=0.7748; P=0.0089) mientras que para P. brevifrons no es significativa (R2=0.09; P=0.51). Esto podría indicar que la humedad relativa es un factor limitante para P. erythropleura. La especie P. palmeri, común en BST y M, reveló para BST una tendencia no significativa (TA: R2=0.48; P=0.08; HR: R2=0.47; P=0.08), pero que sugiere una mayor abundancia en función a una mayor temperatura ambiente y humedad relativa, mientras que para M esta misma especie no presenta tal tendencia. Al analizar esta especie en los dos ambientes de manera conjunta no se observó ninguna tendencia (TA: R2=0.11; P=0.46; HR: R2=0.16; P=0.37).
Por otra parte, la humedad relativa respecto a la temperatura del aire en el momento de la captura de cada individuo, para un rango entre 15.5 y 18.5 ºC, mostró un valor máximo de 92.5% aproximadamente a los 16.7ºC (R2=0.3877; P<0.0001) para una regresión cuadrática. Esta interacción señala que la abundancia máxima al momento de captura de las especies estudiadas se alcanza en una humedad relativa con valores cercanos a los máximos. El 60% de los individuos (38/63) se capturaron cuando los valores de Humedad relativa variaron entre 84 y 100%, para este mismo porcentaje de captura la temperatura sólo varió entre 16.2 y 16.9 ºC. Se registró el 46% (22/48) de todos los individuos de las tres especies más abundantes (P. palmeri, P. brevifrons y P. erythropleura) a una temperatura del aire máxima de 16.7°C y una humedad relativa máxima de 94.6% (R2=0.5626; P<0.0001).
La evaluación de aspectos estructurales de la vegetación relacionada con la abundancia de individuos sugiere que las especies estudiadas tienen preferencias de hábitat significativamente diferentes (X 2 = 53.1 P< 0.001). Del valor total del Chi cuadrado el 82% lo aportaron las especies P. palmeri, P. calcaratus y P. thectopternus. Las dos últimas tienen preferencias opuestas a P. palmeri. Esto sugiere la existencia de tres tipos diferentes de preferencias estructurales en el grupo de anuros respecto a los siguientes parámetros vegetales: cobertura vegetal (%), altura promedio (m) del estrato subarbóreo (Ar), densidad de este estrato (ind/m2), densidad (ind/m2) del estrato arbustivo (ar) y la capa de hojarasca (cm.). En primer lugar, se agruparon las especies con menor aporte al valor total de Chi-cuadrado (18%): P. brevifrons, P. erythropleura y “E”. mantipus, y por otro lado, dos grupos más, con las especies P. calcaratus, P. thectopternus en uno y P. palmeri en otro.
En segundo lugar, considerando las variables altura promedio (m) del estrato arbóreo inferior (Ai), altura promedio (m) del estrato arbustivo (ar) y densidad (ind/m2) del estrato arbóreo inferior (Ai), se detectaron dos agrupamientos, uno con cuatro especies (P. brevifrons, P. erythropleura, “E”. mantipus, y P. palmeri) y el otro integrado por P. calcaratus y P. thectopternus. En la Tabla 7 se muestra que las especies del grupo I toleran más los ambientes medianamente intervenidos que las del grupo II, presentes en ambientes más conservados. En cambio, P. palmeri está en ambientes mediana y altamente intervenidos.
Este estudio determinó la distribución de especies de anuros en áreas con diferentes grados de alteración principalmente en períodos de tiempo de poca pluviosidad, lo cual no permite una extrapolación de su comportamiento teniendo en cuenta los picos estacionales del año. Igualmente, aunque se necesitan una mayor cantidad de datos para tener una mejor explicación de las relaciones de este grupo de animales con las variables microambientales, los resultados indican que los anuros seleccionan remanentes de bosque con una alta cobertura vegetal, amplia capa de hojarasca, alta humedad relativa y bajas temperaturas de aire y suelo. La información obtenida es importante para programas de conservación de los anfibios, al igual que de los bosques donde estas habitan, los cuales deben ser complementados con estudios de historia natural de las especies, de diversidad genética y estado de las poblaciones, así como la creación de corredores que permitan la interacción entre los organismos de los fragmentos.
AGRADECIMIENTOS
Agradecemos por la financiación de esta investigación a Idea Wild y a la Fundación Azul y Verde, especialmente a su director Luis Hernando Rincón, a Germán Morales y a Zaida Rincón. Igualmente, deseamos agradecerles a los evaluadores del manuscrito.
LITERATURA CITADA
1. Blaustein, A. & D. Wake. 1995. Declive en las poblaciones de anfibios. Investigación y Ciencia 225: 8-13. [ Links ]
2. Camero, E. 1999. Estudio comparativo de la fauna de coleópteros (Insecta: Coleoptera) en dos ambientes de bosque húmedo tropical colombiano. Revista Colombiana de Entomología 25: 131-135. [ Links ]
3. Castro, F. 1988. Ecología de una comunidad de lagartos Anolis del bosque pluvial tropical de la costa Pacífica colombiana. Doctoral Dissertation. North Texas State University. Denton, Texas. 99 pp.
4. Collins, J. & A. Storfer. 2003. Global amphibian declines: Sorting the hypotheses. Diversity Distribution 9: 89–98. [ Links ]
5. Crump, M. & N. Scott. 1994. Visual encounter surveys. Pp. 84-92 in R. Heyer, M. Donnelly, R. McDiarmid, L. Hayek, and M. Foster (eds.), Measuring and Monitoring Biological Diversity: standard methods for amphibians. Smithsonian Institution Press. Washington. [ Links ]
6. Donnelly, M. 1998. Potential effects of climate change on two neotropical amphibian assemblages. Climatic Change 39: 541-561. [ Links ]
7. Heinicke, M., W. Duellman & B. Hedges. 2007. Major Caribbean and Central American frog faunas originated by ancient oceanic dispersal. Proceedings of the National Academy of Science 104 (24): 10092-10097. [ Links ]
8. Holdridge, L. 1996. Ecología basada en Zonas de Vida. Instituto Interamericano de Cooperación para la Agricultura. San José, Costa Rica. 216 pp. [ Links ]
9. García-R., J., F. Castro-H. & H. Cárdenas-H. 2005. Relación entre la distribución de anuros y variables del hábitat en el sector La Romelia, Parque Nacional Natural Munchique (Cauca, Colombia). Caldasia 27 (2): 299-310. [ Links ]
10. Lips, K. 1998. Decline of a tropical montane amphibian fauna. Conservation Biology 12: 106–117. [ Links ]
11. Lynch, J. D. & W. E. Duellman. 1997. Frogs of the genus Eleutherodactylus in western Ecuador: systematics, ecology, and biogeography. The University of Kansas Natural History Museum, Special Publication, 23: 1-236. [ Links ]
12. Karr, J. & R. Roth. 1971. Vegetation structure and avian diversity in several new world areas. American Naturalist 105: 423-435. [ Links ]
13. MICROSOFT OFFICE. 2003. Microsoft Excel. Microsoft Corporation. [ Links ]
14. Parris, M. 1999. Review: amphibian surveys in forest and woodlands. Contemporary Herpetology 1: 1-14. [ Links ]
15. Pearman, P. 1997. Correlates of Amphibian diversity in an altered landscape of Amazonian Ecuador. Conservation Biology 11 (5): 1211-1225. [ Links ]
16. Pounds, J. & M. Crump. 1994. Amphibian declines and climatic disturbance: the case of the golden toad and the harlequin frog. Conservation Biology 8: 72-85. [ Links ]
17. Pounds, A., M. Bustamante, L. Coloma, J. Consuegra, M. Fogden, P. Foster, E. Lamarca, K. Masters, A. Merino, R. Puschendorf, S. Ron, A. Sanchez, C. Still & B. Young. 2006. Widespread amphibian extinctions from epidemic disease driven by global warming. Nature 439 : 161-167. [ Links ]
18. Rangel-Ch., J.O. & A. Velásquez. 1997. Métodos de estudio de la vegetación. Pp. 59-87 en: O. Rangel, P. Lowy y M. Aguilar (eds.), Colombia Diversidad Biótica II: Tipos de vegetación en Colombia. Instituto de Ciencias Naturales-Universidad Nacional de Colombia. Bogotá. [ Links ]
19. Rangel-Ch., J.O. & G. Lozano. 1986. Un perfil de vegetación entre la Plata (Huila) y el volcán Puracé. Caldasia 68-70: 503-547. [ Links ]
20. Rincón, F. & F. Castro. 1998. Aspectos ecológicos de una comunidad de Eleutherodactylus (Anura: Leptodactylidae) en un bosque de niebla del occidente de Colombia. Caldasia 20: 193-202. [ Links ]
21. Sokal, R. & J. Rohlf. 1969. Biometria. W. H. Freeman and Company. New York. [ Links ]
22. Statsoft. 2001. STATISTICA: Data Análisis Software System, version 6.0. StatSoft, Oklahoma. [ Links ]
23. Urbina, J. & M. Londoño. 2003. Distribución de la comunidad de herpetofauna asociada a cuatro áreas con diferente grado de perturbación en la isla Gorgona, Pacífico colombiano. Revista Colombiana de Ciencias Exactas, Físicas y Naturales 27: 105-113. [ Links ]
24. Vargas, F. & F. Castro. 1999. Distribución y preferencias de microhábitat en anuros (Amphibia) en bosque maduro y áreas perturbadas en Anchicayá, Pacífico colombiano. Caldasia 21: 95-109. [ Links ]
25. Vargas, F. & M. Bolaños. 1999. Anfibios y reptiles presentes en hábitats perturbados de selva lluviosa tropical en el bajo Anchicayá, Pacífico Colombiano. Revista Colombiana de Ciencias Exactas, Físicas y Naturales. Suplemento Especial 23: 499-508. [ Links ]
26. Young, B., K. Lips, J. Reaser, R. Ibañez, A. Salas, J. Cedeño, A. Coloma, S. Ron, E. La Marca, J. Meyer, A. Muñoz, F. Bolaños, G. Chaves & D. Romo. 2001. Population declines and priorities for amphibian conservation in Latin America. Conservation Biology 15: 1213-1223. [ Links ]
Recibido: 07/03/2007
Aceptado: 27/04/2007